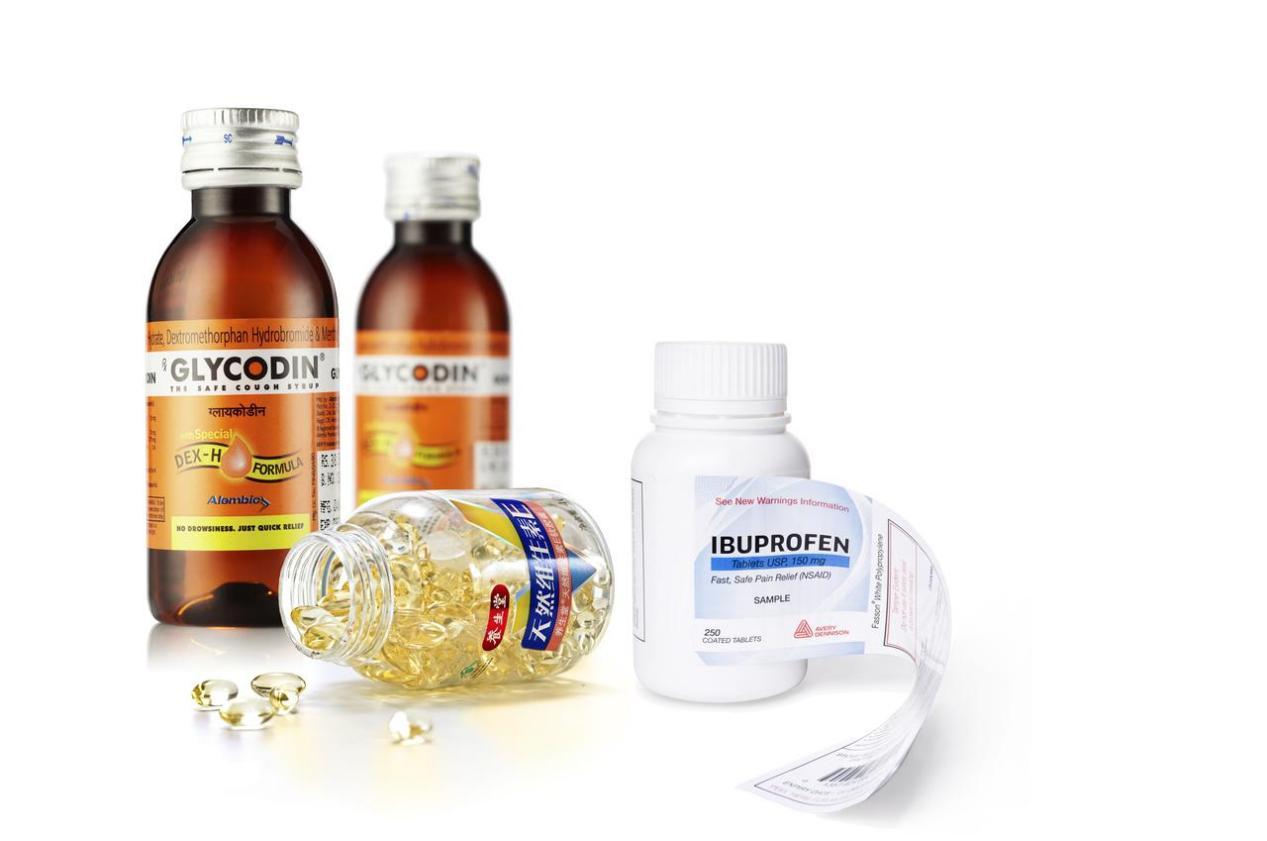
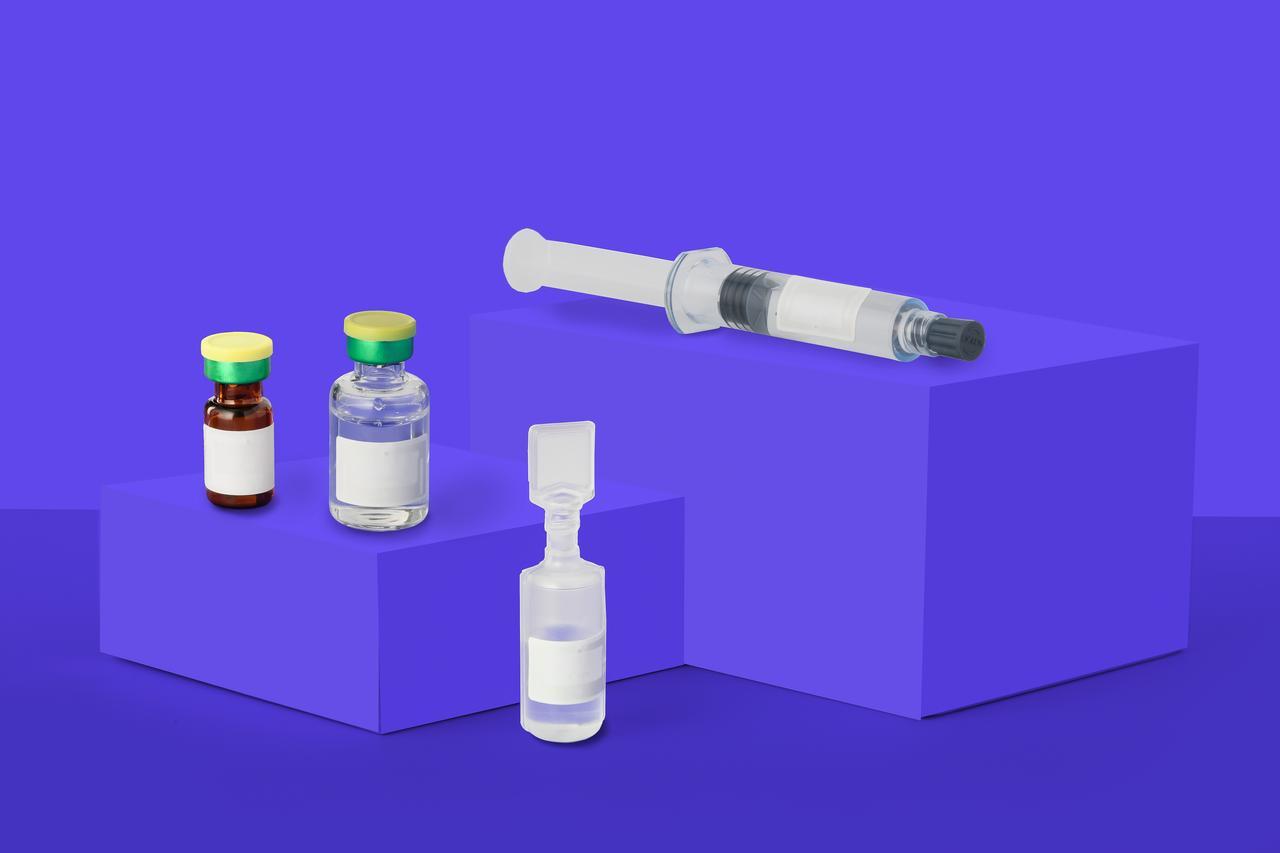
注射球表面小、易弯曲,标签需要抗冷凝、防起翘
血袋标签需要耐低温并弯曲,并符合医药接触标准
贴近药液的塑料容器,则需低迁移材料避免成分渗透
等等......
这背后,没有“标准答案”,而是对标签材料+包装结构+药品特性+贴标工艺+法规要求的全方位匹配。
🧭持久可用,才是真的“安全合规”
在医药行业,一次标签材料选择,可能伴随产品使用长达10年以上。
任何微小调整(比如更换底纸或粘合剂)都可能重新引发一轮完整的合规流程,甚至推迟产品上市。
“标签不仅要现在合规,更要长期稳定可获取,真正降低未来风险。”
—— Gabriela Gregor
因此,我们在材料选择上坚持“全生命周期”视角,优先考虑那些在数据、认证、供应链等方面都具备长期保障的方案。
全球药企的本地落地,靠的是“双轮驱动”
Gabriela还指出:“许多全球药企在欧洲做完标签认证后,进入亚太或中国市场时仍面临挑战。”
不同地区的法规要求、贴标设备、储运环境都可能不同,即使材料规格一致,也可能需要重新验证或微调。
这时,艾利丹尼森的全球服务体系+本地技术支持就发挥出独特优势——我们不仅有全球一致的材料标准,也有中国本地的团队和服务资源,帮助客户在落地时确保方案真正可行、合规、稳妥。
面向中国市场,我们准备好了
随着中国医药产业迈向更高标准的质量与监管水平,对标签系统的专业性与可持续性也提出了全新要求。
艾利丹尼森正将在欧美市场积累的标签经验与专业方案,逐步引入中国市场。我们愿携手本地药企、包装商、印刷厂,共同推动中国医药包装在安全性、稳定性与合规性上的再升级。